初中化学第九单元四个考点知识点归纳总结,预习或复习必备。
本章主要是学习溶解现象,认识溶液、溶剂、溶质等概念,为后续的溶液计算做铺垫。其次,对于一些常见的乳化现象,我们也需要有充分的了解。最后,我们探索了几种物质在水溶液中溶解时的温度变化。这个实验过程可以帮助学生掌握研究饱和与不饱和溶液相互转化的因素。其中,学习难点主要集中在乳化和溶解的区别,以及如何从微观角度分析溶解过程中的放热和吸热现象。
1.溶液、饱和溶液和不饱和溶液的形成

溶液的相关量中有溶质、溶剂和溶液。如何区分它们?以及它们的概念是什么,这是我们解决方案学习最基本的内容。相比之下,许多学生应该打破传统的溶剂和溶质溶液之间的区别概念的理解。溶质不一定是固体,也可以是液体或气体。
同时,为了加深人们对溶液的理解,首先要了解溶液和混合溶液的区别,两种状态下它们的本质区别在哪里?这是我们掌握解法首先要解决的问题。

在学习过程中,物质溶解过程中会发生吸热或放热现象,主要是因为溶解过程中发生了两种变化。一种是溶质的分子或离子在水的作用下分解,像水扩散时,这个过程需要吸热,另一种是溶质的分子或离子和水分子合成水分子放热。当扩散过程中吸收的热量小于水和粒子合成释放的热量时,表示为温度的高低。否则,溶液的温度会降低。在这个过程中,溶液从环境中吸收或释放热量。

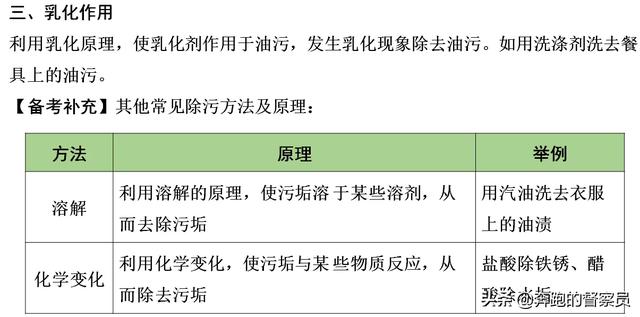

首先,我们可以从它的概念来判断饱和溶液和不饱和溶液的区别。判断的方法主要是根据现有溶液状态下加入融资后是否有沉淀,或者加入的溶质是否继续溶解来判断饱和与不饱和状态。

而且在这种状态下,它有一个前提,就是温度不变时,即温度变化时,饱和溶液可以像不饱和溶液一样相互转化。

二、试验部位、溶解度和溶解度曲线

溶解度主要用于研究饱和与不饱和溶液的两种相对状态。在研究过程中,我们假设在一定的溶剂量和一定的温度下,不饱和溶液和饱和溶液之间存在相关性。如果前提是变化之后,那么饱和度和不饱和度的研究就没有实际意义和参考价值了。



溶解度曲线实际上是在研究饱和溶液和不饱和溶液的过程中,不确定因素和温度在变化时,溶质溶解度的变化过程。在这个过程中,当温度变化时,溶解度的变化趋势决定了溶质在溶解过程中是放热还是吸热。当两条溶解度曲线相交时,交点和对应的温度是大家要注意的重要信息。

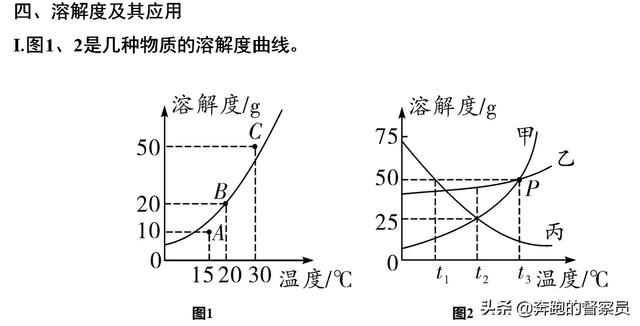
溶解度曲线的应用是中考化学的重要考点之一,考察形式也是近年来的热点。因此,学生应该学会理解溶解度曲线的图像,并能够提取对我们解题有用的信息。考察的点也应该主要集中在以下七个考点,每个考点都可以从图像中获取信息,大家在学习的时候可以把每个考点在图形中展示出来,这样对溶解度曲线的理解就更全面了。






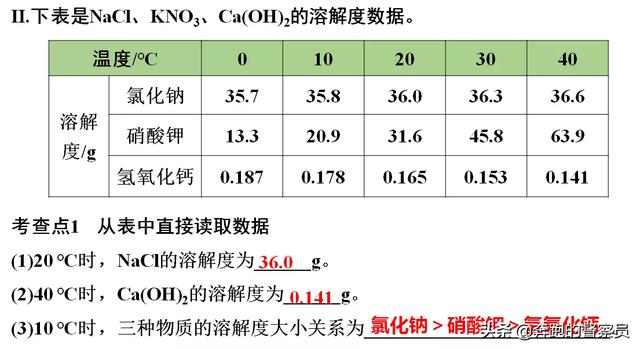

三、溶质质量分数的计算



第四,溶液的制备
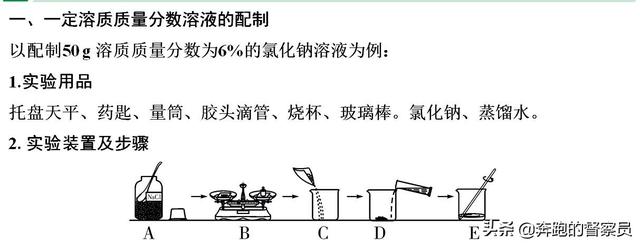
溶液配制是初中化学计算中最重要的考点之一。考察的形式是将一定比例的液体配制成另一比例的溶液。在这个过程中,除了计算,还要谨慎对待实验的操作过程。每个步骤的细节都要注意。对于整个实验的合理性和操作步骤的符合性,可以在考试中单独组成考点进行考察。

总之,在初中化学第九单元关于溶液的学习过程中,除了对其概念有更深的理解外,溶液配制和溶解度曲线考点的分析和总结是大家学习的重点和难点。溶解度曲线可以通过数形结合来理解,其复习效率更高。