导读
近日,美国胃肠病协会(AGA)在Gastroenterology杂志上发布了卟啉病的临床指南。以下是该指南中急性肝卟啉病的病理生理、诊断和治疗部分。
病理生理学
急性肝卟啉病(acute hepatic porphyrias,AHPs)属于先天性的血红素合成异常,包括急性间歇性卟啉病(AIP)、遗传性粪卟啉病(HCP)、混合型卟啉病(VP)和罕见的常染色体隐性遗传5-氨基乙酰丙酸脱水酶缺乏卟啉病(ALADP),所有类型的AHPs均表现为代表性酶的缺陷,致使患者容易在特定诱发因素下出现具有神经毒性的卟啉前体异常高水平蓄积而发病。主要累及神经系统,均可出现临床上难以鉴别的急性神经症状,还可能存在多系统受累,包括皮肤、肝脏和肾脏。
AIP、HCP和VP分别由PBGD、CPOX或原卟啉原氧化酶缺陷导致,并由肝血红素合成途径的第一个关键酶酶——ALA合成酶(ALAS1)的过度活性促进(见图1)。
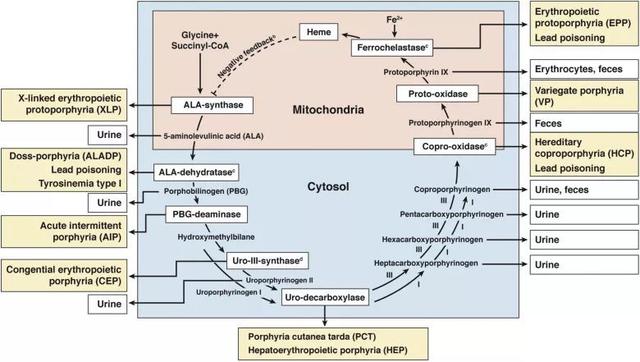
图1 血红素的生物合成
外源性物质、吸烟、过量饮酒、节食、雌激素、以及细胞色素P450(CyP450),均可诱导产生ALAS1。
ALAS1的明显诱导将造成ALA和PBG的生成增加和蓄积,后两者可以导致急性神经症状发作——不过,目前还不清楚ALA和PBG是否是相关的神经毒素。酶缺陷下游卟啉的反常增加,显然是由ALA的诱导合成和PBG的过度积累介导的,在临床上与严重病例的尿液呈红色或变暗相对应。
临床表现
AHPs通常不会在青春期之前发作。一些AHPs的女性患者随月经周期出现周期性发作,尤其是在孕激素水平最高的黄体期,并随着月经开始而缓解。
通常,患者会出现间歇性腹部绞痛,可以延伸到背部和四肢,且时常伴有便秘、恶心、呕吐、肠梗阻和感觉异常等症状。心动过速合并高血压和深红色尿液(图2A),可作为进一步的诊断体征。急性卟啉症发作时的疼痛通常是逐渐显现的,通常伴有典型的前驱症状,经过数小时逐步加重并持续数天。有些患者的疼痛主要发生在胸部、背部或四肢,但更常见的表现是严重的腹痛。
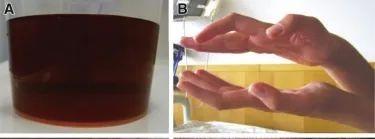
图2 AHP的临床症状。A:深红色尿液,在空气/氧气下进一步变黑;B:首发表现后,手部伸肌出现运动神经病。
当被误诊或治疗不当时(如低热量营养、疼痛治疗不足导致患者压力增加),患者可能逐渐发展为周围运动神经病变,首先影响上肢近端,可能进展为手部及臂部伸肌瘫痪(图2B)、四肢轻瘫、以及呼吸骤停。
有些患者会表现出焦虑、混乱和过度兴奋,包括幻觉产生、精神错乱或癫痫发作。抗利尿激素分泌不当(Schwartz–Bartter综合征)会导致顽固性低钠血症,这是急性卟啉症的另一个临床症状,可能危及生命。
随着疾病频繁发作,高血压性肾损害和肝细胞癌的风险增加。一种肾肽转运体2(PEPT2*1*)的变体对ALA具有很高的亲和力,并促进其再吸收,其可能导致肾损伤。PEPT2*1也存在于脉络膜丛中,可能在向大脑泵入毒性ALA的过程中起重要作用,这可以解释患者对神经精神症状的易感性。
HCP和VP也可引起皮肤光敏,而AIP只有在严重肾脏疾病导致卟啉进一步积累时才会发生。
在AIP患者中,有多达5%的患者会复发。
诊断
表1 AHPs的诊断和临床特征
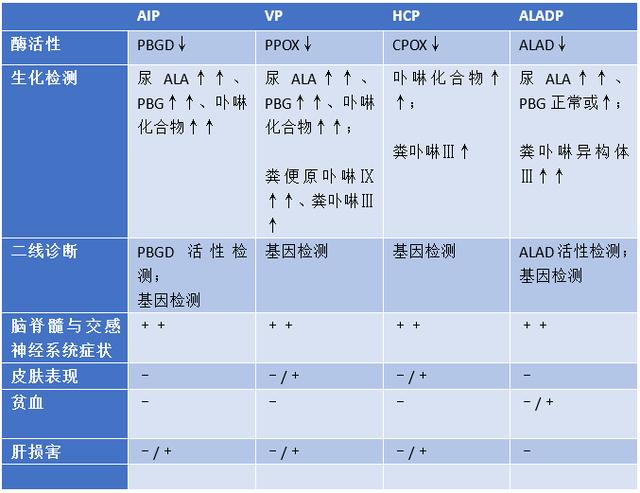
需采集患者随机尿进行卟啉及其前体的分析(见表1)。
尿液中ALA和PBG增加4倍以上,可用于鉴别AIP/VP与HCP患者。罕见性ALADP或铅中毒患者中,在尿PBG没有显著增加的情况下,尿液中ALA的含量可增加10倍以上(表1)。
通过基因测序明确具体突变可进一步确保诊断。
由于个别病例和疾病分期可能有不同的模式,而且由于卟啉症的相对罕见性和复杂性,最终的评估应由卟啉症中心的专家进行(www.porphyriafoundation.com,www.porphyria.uct.ac.za,www.porphyria.eu)。
无症状患者也建议每年进行一次检查。如果尿液分析发现急性(肝)卟啉症,有必要测量红细胞中PBGD的活性并进行遗传分析,以确定诊断AIP。
了解患者的突变情况后,可以对其所有一级亲属进行针对性的遗传分析,以确定无症状的携带者,并向他们告知卟啉症的诱因。值得注意的是,95%的基因携带者终生无症状。
治疗
AHPs有特定的治疗方法(见表2)。
表2 急性卟啉病的治疗
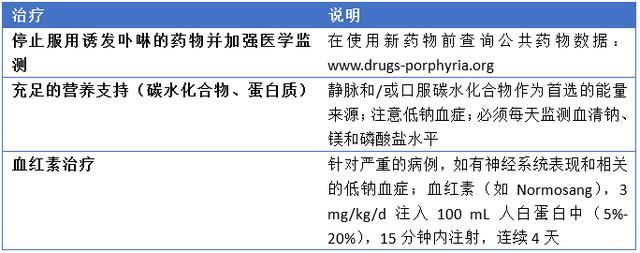
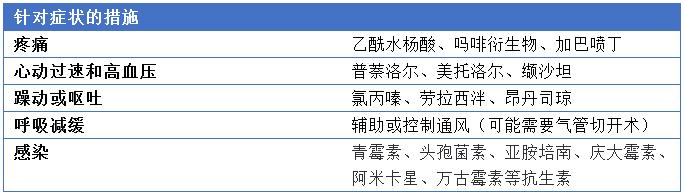
充足的热量支持(碳水化合物、蛋白质)对于AHP的治疗至关重要。低钠血症患者应接受血红素治疗,因为低钠血症合并葡萄糖输液可使病情恶化。
疼痛应立即处理并严格预防。疼痛压力会导致神经内分泌反应,从而激活ALAS1,加重症状。耐受性良好的药物,如阿片类药物和加巴喷丁(gabapentin),它们不会在肝脏中诱导ALAS1,并通过肾脏排出。此外,如果长时间的误诊,可能导致患者焦虑、抑郁,需要心理治疗,辅以抗抑郁或抗焦虑药物。

周期性发作的患者(每年超过3例)经常接受预防性血红素治疗(间隔治疗)。
然而,由于血红素降解产物与内皮细胞、血小板和凝血因子结合,频繁的血红素灌注常常导致静脉闭塞。通过血红素联合白蛋白给药,可减轻副作用。应避免高频率的血红素注入。
总之,严格消除日常生活中的诱发因素仍然是预防和治疗的主要措施。
新型药物Givosiran是一种皮下使用的N-乙酰半乳糖胺结合RNA干扰治疗,处于研究阶段的,以肝脏ALAS1为靶点。临床前研究表明, 应用Givosiran可使AIP小鼠的肝ALAS1沉默,从而预防和治疗急性发作。Ⅲ期临床试验正在进行中。
最后一种选择是肝移植。在严重的、致残的、高铁血红素治疗无效的难治性患者中原位肝脏移植确实有效,且已有成功案例。由于原位肝移植存在相关的病死率,仅作为最后的治疗手段。来自英国的10名肝移植成功的患者得到了生化指标和症状的改善,但有4例发生肝动脉血栓形成,因此,建议移植后抗凝。
参考来源:https://doi.org/10.1053/j.gastro.2019.04.050